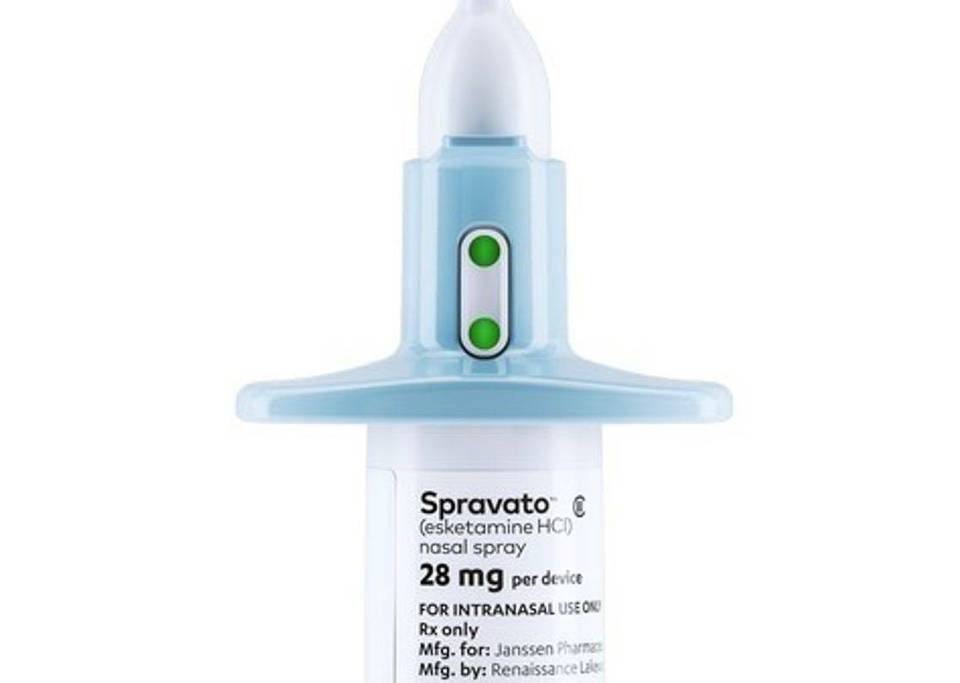
Estados Unidos aprovam antidepressivo em forma de spray nasal

EMS celebra 55 anos de história com novo posicionamento de marca
1 de março de 2019
Três pessoas já teriam se curado de HIV no mundo, anunciam médicos
11 de março de 2019Estados Unidos aprovam antidepressivo em forma de spray nasal
Remédio de ação rápida tem substância derivada de anestésico; especialistas receberam notícia com cautela por causa de resultados em estudos
6.mar.2019 às 20h09
Dos 16 milhões de adultos que sofrem de depressão nos Estados Unidos, um quarto ou mais obtém pouco ou nenhum benefício dos tratamentos disponíveis, quer medicamentos, quer psicoterapia. Na terça-feira (6), a Food and Drug Administration (FDA), agência americana de fiscalização e regulamentação de alimentos e remédios, aprovou um medicamento vendido sob receita que pode ajudar essa população: um remédio de ação rápida derivado de um anestésico disponível há muito tempo e de uso generalizado, a cetamina.
A aprovação representa a transição para uma nova geração de medicamentos antidepressivos, depois da era Prozac.
O tratamento aprovado, um composto chamado “esketamine”, é um spray nasal desenvolvido pela Janssen Pharmaceuticals, subsidiária do grupo Johnson & Johnson, e será comercializado sob a marca Spravato. O remédio contém uma porção ativa da molécula da cetamina, cujas propriedades antidepressivas não são bem conhecidas até o momento.
“Ainda bem que agora temos algo com um mecanismo de ação diferente do que é usado em antidepressivos anteriores”, disse Erick Turner, ex-avaliador de medicamentos da FDA e professor associado de psiquiatria na Universidade de Saúde e Ciência do Oregon. “Mas encaro o entusiasmo quanto a isso com ceticismo, porque nosso mundo é como quando Lucy segura a bola de futebol americano para Charlie Brown chutar: ela sempre acaba tirando a bola do lugar, por mais esperança que tenhamos”.
O anestésico genérico já está disponível com frequência cada vez maior como tratamento contra depressão em centenas de clínicas nos Estados Unidos que oferecem tratamentos intravenosos para pacientes deprimidos. Alguns estudos apontam que seu uso pode beneficiar pacientes resistentes a outros tratamentos. A cetamina frequentemente causa sensações de alucinação, quando administrada; nas décadas de 1980 e 1990, ela era popular como droga, usada por frequentadores de casas noturnas e conhecida como Special K.
A dosagem recomendada do remédio recém-aprovado é duas aplicações por semana durante quatro semanas, com doses se requeridas se requeridas, e em companhia de um dos antidepressivos de uso oral usados comumente. A aprovação da FDA requer que as doses sejam aplicadas numa clínica ou consultório médico, e que os pacientes sejam acompanhados por pelo menos duas horas, com registro de suas experiências. Os pacientes não devem dirigir no dia do tratamento.
A “esketamine”, como a cetamina, pode ser usada de forma abusiva, e os dois medicamentos podem causar episódios psicóticos em pessoas que correm risco elevado desse tipo de reação. A monitoração de segurança requer que os médicos tenham um espaço reservado ao acompanhamento dos pacientes, o que pode representar um desafio logístico, disseram alguns psiquiatras.
O custo de um tratamento como esse no atacado será de entre US$ 2,36 mil e US$ 3,54 mil, de acordo com a Janssen, e especialistas dizem que isso dará à empresa uma fatia do mercado mundial de antidepressivos, que movimenta US$ 12 bilhões ao ano e no qual os medicamentos genéricos dominam, hoje.
A aprovação da “esketamine” marca uma nova abordagem no tratamento de sérios distúrbios de humor, dizem especialistas. O Prozac e medicamentos semelhantes reforçam a ação de mensageiros cerebrais como a serotonina; são moderadamente efetivos, mas demoram semanas ou meses a fazer efeito e, no caso de muitos pacientes, não aliviam muito a depressão.
Em contraste, os compostos baseados em cetamina —há diversos deles em desenvolvimento —começam a fazer efeito em poucas horas ou dias, e são efetivos em algumas pessoas classificadas como “resistentes a tratamento”, o que significa que elas já usaram outros antidepressivos e não se beneficiaram deles.
Especialistas com longa experiência no tratamento de depressões receberam a notícia positivamente, mas continuam cautelosos. A efetividade da categoria anterior de antidepressivos, como o Prozac e o Paxil, foi imensamente exagerada quando os produtos chegaram ao mercado. E os resultados dos testes com a “esketamine”, pagos e conduzidos pela Janssen, foram contraditórios.
Em cada teste examinado, todos os pacientes começaram um tratamento com um novo antidepressivo e ao mesmo tempo um tratamento paralelo com “esketamine” ou um placebo. Em um estudo de um mês de duração, os pacientes que receberam a “esketamine” apresentaram resultados estatísticos melhores do que os pacientes que receberam o placebo, com redução de 21 pontos em sua marca na escala padrão de 60 pontos usada para avaliar a depressão, ante 17 pontos de redução para os participantes que receberam o placebo.
Mas em dois outros testes, o medicamento não apresentou desempenho estatístico superior ao do placebo. Historicamente, a FDA requer que um remédio obtenha sucesso em dois testes clínicos curtos antes de aprová-lo. A agência adotou um critério menos severo para a “esketamine”, optando em lugar disso por estudar reincidência nos pacientes que se saíram bem com o novo tratamento.
No teste de reincidência, a Janssen reportou que apenas um quarto dos participantes mostraram recaídas, ante 45% dos participantes que receberam o placebo. Todos os pacientes haviam recebido um diagnóstico de depressão resistente a tratamento, ou DRT, depois de passarem por diversas rodadas mal sucedidas de tratamento com remédios.
“Não tivemos novidade alguma em 30 anos”, disse Steven Hollon, professor de psiquiatria e ciências do comportamento na Universidade Vanderbilt. “Assim, se esse remédio é uma forma efetiva de obter resposta mais rápida em pessoas que resistem a tratamentos, e se pudermos usá-lo em segurança, será um grande avanço”.
Leia mais em: https://www1.folha.uol.com.br/equilibrioesaude/2019/03/estados-unidos-aprovam-antidepressivo-em-forma-de-spray-nasal.shtml